Описание
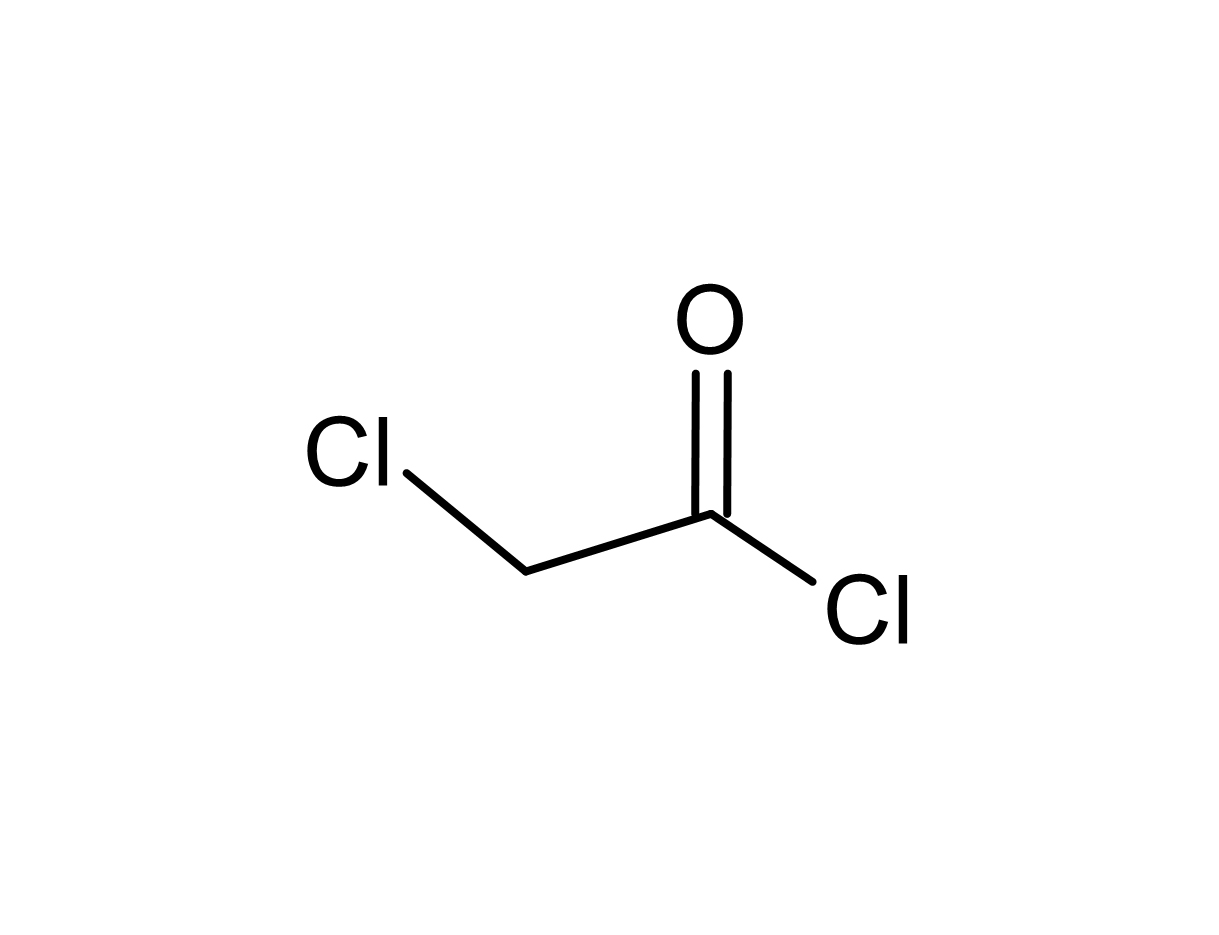
Хлороацетилхлорид: свойства, получение и применение
Хлороацетилхлорид является хлорированным ацилхлоридом, обладающим бифункциональными свойствами. Это делает его ценным химическим материалом, используемым в различных областях.
Основные характеристики
Хлороацетилхлорид представляет собой бесцветную или слегка желтоватую жидкость с резким запахом. Во влажной среде он дымит, образуя соляную кислоту.
Методы получения
На промышленном уровне хлороацетилхлорид получают путем карбонилирования метиленхлорида, окисления винилиденхлорида или в результате реакции между хлором и кетеном. В лабораторных условиях его можно получить путем реакции хлоруксусной кислоты с пентахлоридом фосфора или тионилхлоридом.
Реакции
Благодаря своим бифункциональным свойствам, хлороацетилхлорид легко образует сложные эфиры и амиды, а также способен образовывать другие связи, например, с аминами. Отметим, что он активно используется в синтезе лидокаина.
Применение
Хлороацетилхлорид применяется в основном как промежуточное звено при производстве гербицидов семейства хлорацетанилидов, включая метолахлор, ацетохлор, алахлор и бутахлор. Ежегодно используется около 100 миллионов фунтов этого вещества. Кроме того, он используется для производства хлорацетофенона, другого химического промежуточного продукта, который также применяется в качестве слезоточивого газа. Синтез хлорацетофенона осуществляется методом ацилирования бензола по Фриделю-Крафтсу с использованием хлорида алюминия в качестве катализатора.
В нашем магазине ‘Уральский химик’ вы можете приобрести хлороацетилхлорид и другие химические реагенты для ваших нужд.